Investigaciones
Nueva combinación para el tratamiento de la hepatitis C con precio accesible muestra una tasa de curación del 97%
DNDi, 12 de abril de 2018
https://www.dndi.org/2018/media-centre/langues-press-releases/nueva-combinacion-para-el-tratamiento-de-la-hepatitis-c-con-precio-accesible-muestra-una-tasa-de-curacion-del-97/
Los resultados hacen accesibles un tratamiento de salud pública para la hepatitis C
Se ha demostrado que un tratamiento combinado de hepatitis C, a precio más accesible, que incluye el nuevo fármaco candidato ravidasvir, es seguro y eficaz, con tasas de curación extremadamente altas para los pacientes, inclusive en casos difíciles de tratar, según los resultados provisionales del ensayo de Fase II / III STORM-C-1, expuestos por la Iniciativa de Medicamentos para Enfermedades Olvidadas (Drugs for Neglected Diseases Iniciative DNDi), organización de investigación y desarrollo sin fines de lucro, en la– Conferencia Internacional del Hígado (International Liver Conference) en París.
“Los resultados indican que la combinación sofosbuvir / ravidasvir es comparable a las mejores terapias contra la hepatitis C disponibles en la actualidad, pero con un precio más accesible, lo que viabilizaría una opción alternativa en países excluídos de programas de acceso de compañías farmacéuticas“, dijo Dr Bernard Pécoul, director ejecutivo de DNDi.
El ensayo clínico con los medicamentos producidos por el fabricante egipcio Pharco Pharmaceuticals fue administrado por DNDi y copatrocinado por el Ministerio de Salud de Malasia, en diez localidades de Malasia y Tailandia. Los acuerdos firmados en 2016 y 2017 que permitieron los ensayos clínicos y la ampliación del número de pacientes en Malasia establecieron un precio target de 300 USD para un tratamiento de 12 semanas, una disminución de casi 100% en comparación con los precios de tratamientos ya existentes en Malasia.
“Como la hepatitis C se ha convertido en un grave problema de salud pública en Malasia, es crucial aumentar el acceso al tratamiento en beneficio de la nación”, dijo Datuk Dr Noor Hisham Abdullah, director general de salud del Ministerio de Salud de Malasia. En septiembre de 2017, el gobierno de Malasia emitió una licencia de “uso gubernamental” para las patentes de sofosbuvir, permitiendo que 400.000 pacientes afectados por la hepatitis C en Malasia tengan acceso a tratamientos genéricos del VHC (Virus de Hepatitis C) en hospitales públicos.
DNDi realizó el ensayo clínico abierto STORM-C-1 para evaluar la eficacia, seguridad, tolerancia y farmacocinética del fármaco candidato ravidasvir combinado con sofosbuvir. Fueron tratados 301 adultos con infección crónica con la combinación de ravidasvir/sofosbuvir durante 12 semanas para pacientes sin cirrosis hepática y durante 24 semanas para aquellos con cirrosis compensada. De acuerdo con los estándares internacionales que definen la cura para los tratamientos de VHC, 12 semanas después de la finalización del tratamiento el 97% de las personas incluidas estaban curadas (IC 95%: 94.4-98.6). Las tasas de curación fueron muy altas incluso con los pacientes más difíciles de tratar: personas con cirrosis hepática (96% curados), pacientes con VIH realizando su tratamiento habitual (97%), personas infectadas con genotipo 3 (97%) inclusive aquellos con cirrosis (96%) y pacientes que fueron expuestos a tratamientos anteriores contra el VHC (96%). Es importante destacar que los pacientes que combinaban varios de estos factores de riesgo se curaron y no se detectaron factores indeseados de falta de seguridad.
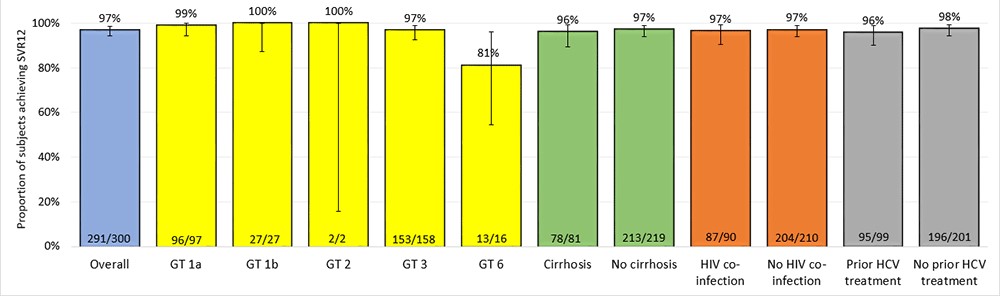
STORM-C-1: Tasas de SVR12 globales y por subgrupos predefinidos – análisis de intención de tratar
“Desde la perspectiva de un proveedor de tratamientos, esto resulta muy interesante, pues estábamos a la espera de un tratamiento simple, con precio más accesible y robusto, tolerado por todos los grupos de pacientes, inclusive los que actualmente obtienen menos resultados, como los pacientes bajo tratamiento antiretroviral”, dijo Pierre Mendiharat, director de operaciones adjunto de Médicos Sin Fronteras (MSF). “Esto será crucial para expandir el tratamiento a los grupos más vulnerables en los países en desarrollo”. MSF y DNDi están trabajando conjuntamente para ampliar el acceso a la atención y al tratamiento de pacientes infectados con el VHC en países de medianos y bajos ingresos, a través del proyecto STORM-C financiado por la iniciativa Capacidad de Inversión Transformativa (Transformational Investment Capacity TIC) de MSF.
Hay en el mundo más de 71 millones de pacientes con hepatitis C, una enfermedad que causa 400.000 muertes al año. Aunque existen tratamientos extremadamente efectivos desde hace varios años, menos de tres millones de personas tienen acceso a estos tratamientos, siendo que cada año un número mayor de individuos son infectados en comparación con los que tienen acceso a los tratamientos. La OMS definió como objetivo que el 80% de las personas diagnosticadas con el VHC reciban tratamiento para el año 2030.
Ravidasvir es un inhibidor oral de NS5A licenciado para DNDi por Presidio Pharmaceuticals. La mayoría de los pacientes inscriptos en el ensayo clínico llevado a cabo por DNDi en Malasia y Tailandia tenían genotipo 1 (42% de los participantes) o genotipo 3 (53%), lo que confirma la eficacia de la combinación mencionada para estos dos genotipos. Estos genotipos, 1 y 3, son los más prevalentes en América Latina, especialmente en Argentina, Brasil y Chile. Se planean ensayos clínicos adicionales para documentar la eficacia y seguridad de esta combinación en pacientes infectados con otros genotipos de VHC y en grupos particularmente vulnerables, para viabilizar un enfoque de salud pública para el tratamiento de la hepatitis C.
“Pharco se enorgullece de posibilitar un abordaje de salud pública para el tratamiento de la hepatitis C proporcionando tratamientos asequibles. Esperamos continuar colaborando en futuros ensayos clínicos adicionales para confirmar la seguridad y eficacia de ravidasvir”, dijo el Dr. Sherine Helmy, CEO de Pharco.
Referencia del poster
Isabelle Andrieux-Meyer, Tan Soek Siam, Nicolas Salvadori, et al. Seguridad y eficacia de ravidasvir más sofosbuvir, 12 semanas en pacientes no cirróticos y 24 semanas en pacientes cirróticos con los genotipos 1, 2, 3 y 6 del virus de la hepatitis C: el ensayo STORM-C-1 fase II / III. International Liver Congress-Congreso Internacional del Hígado, París, 11-15 de abril de 2018, Francia. Poster LBP-032