Investigaciones
Fluoroquinolonas orales y riesgo de fibromialgia (Oral fluoroquinolones and risk of fibromyalgia)
Saeed Ganjizadeh‐Zavareh, Mohit Sodhi, Tori Spangehl, Bruce Carleton, Mahyar Etminan
British Journal of Clinical Pharmacology 2019, 85:236-239 (acceso libre)
https://bpspubs.onlinelibrary.wiley.com/doi/pdf/10.1111/bcp.13765
Traducido por Salud y Fármacos
Resumen
Recientemente, la FDA incluyó una advertencia de recuadro negro porque las fluoroquinolonas (FQ) pueden provocar síntomas similares a la fibromialgia, pero hasta la fecha no se ha hecho un estudio epidemiológico. Realizamos un estudio de casos y controles utilizando una muestra aleatoria de 9,053.240 sujetos incluidas de la base estadounidense de datos de facturas de salud PharMetrics Plus. Los casos recibieron al menos dos diagnósticos de fibromialgia codificados por un reumatólogo y se aparearon con diez controles seleccionados al azar. Después de identificar 5.148 casos de fibromialgia y 51.480 controles, la relación de tasa ajustada (RR) de fibromialgia asociada con el uso de cualquier fluoroquinolona, amoxicilina y azitromicina fue 1,63 (IC 95%: 1,41–1,87), 1,64 (IC 95%: 1,46–1,85) y 1,68 (IC 95%, 1,49–1,89), respectivamente. El RR ajustado para cualquier uso de FQ en comparación con cualquier uso de amoxicilina o azitromicina fue de 0,99 (IC del 95%: 0,83 a 1,18) y para la azitromicina 0,97 (IC del 95%: 0,82 a 1,16), respectivamente. El riesgo de fibromialgia con FQ es similar al de la amoxicilina y la azitromicina.
Lo que ya se sabe sobre este tema
Las fluoroquinolonas (FQ) son una de las clases de antibióticos más recetadas.
Las series de casos que se han publicado y los casos informados a la FDA han aludido a un mayor riesgo de que al recibir tratamiento con fluoroquinolonas se presenten síntomas similares a la fibromialgia.
Hasta la fecha, ningún gran estudio epidemiológico ha cuantificado este riesgo.
Lo que agrega este estudio
El riesgo de fibromialgia al recibir tratamiento con FQ es similar al riesgo del tratamiento con amoxicilina y la azitromicina.
Este riesgo podría deberse a la afección infecciosa para la cual se prescriben FQ.
Introducción
Las fluoroquinolonas orales (FQ) son una de las clases de antibióticos más recetadas en el mundo. Recientemente, la FDA emitió una advertencia de recuadro negro para las FQ que incluye eventos adversos debilitantes de tipo musculoesquelético [1]. Específicamente, estos eventos se refieren a afecciones discapacitantes relacionadas con tendones, músculos, articulaciones y nervios, y fibromialgia [1]. Las series de casos han descrito como pacientes experimentaron una multitud de eventos adversos mientras recibían tratamiento con FQ, incluyendo síntomas incapacitantes de fatiga, debilidad muscular severa y atrofia similares a la fibromialgia [2]. Estudios recientes han demostrado que podría haber una disfunción mitocondrial subyacente que conectara estas condiciones, especialmente en los trastornos multisintomáticos [2]. La disfunción mitocondrial y la formación de radicales libres pueden causar estrés oxidativo, y el estrés oxidativo a su vez aumenta el daño mitocondrial [2].
Estudios anteriores han detectado que las FQ se asocian a un riesgo elevado de rotura de tendones [3], neuropatía periférica [4] y síndrome del túnel carpiano [5]. Hasta la fecha, no hay ningún estudio epidemiológico que haya evaluado el riesgo de que las FQ se asocien a problemas musculoesqueléticos incapacitantes. Además, dado que las infecciones respiratorias para las que se prescriben FQ también pueden producir fibromialgia [6], no está claro si los eventos adversos musculoesqueléticos informados durante el tratamiento con FQ se deben a la infección o es un efecto de las FQ. Como los eventos adversos relacionados con las FQ se asemejan a la fibromialgia, examinamos el riesgo de fibromialgia asociada a las FQ en un gran estudio epidemiológico.
Métodos
Fuentes de datos y diseño del estudio.
Como principal fuente de datos para este estudio utilizamos una muestra aleatoria de PharMetrics Plus, una gran base de datos de facturas de salud de EE UU. La base de datos contiene las facturas de salud de más de 150 millones de afiliados únicos, e incluye las facturas de los médicos y los gastos en farmacia. Todos los diagnósticos médicos se capturan utilizando la novena y décima edición de la clasificación internacional de enfermedades (ICD ‐ 9 y 10). Contiene todos los medicamentos recetados a pacientes ambulatorios, incluyendo información sobre el nombre del medicamento, la cantidad de dosis dispensada y el suministro diario. La base de datos constituye una representación razonable de todas las áreas geográficas de EE UU [7]. El estudio de casos y controles utilizó una muestra aleatoria de 9,053.240 sujetos que facturaron gastos entre 2006 a 2016. Se eligió un diseño de casos y controles, ya que solo utiliza una muestra de la población (como controles) para estimar la razón de tasas (RR), mitigando las complejidades que pueden surgir de un diseño de cohorte que utilizará una muestra grande de más de 9 millones de sujetos. Se obtuvo la aprobación del comité de ética clínica de la Universidad de Columbia Británica. No fue necesario el consentimiento del paciente ya que este estudio no utilizó datos reales del paciente.
Selección de casos y controles
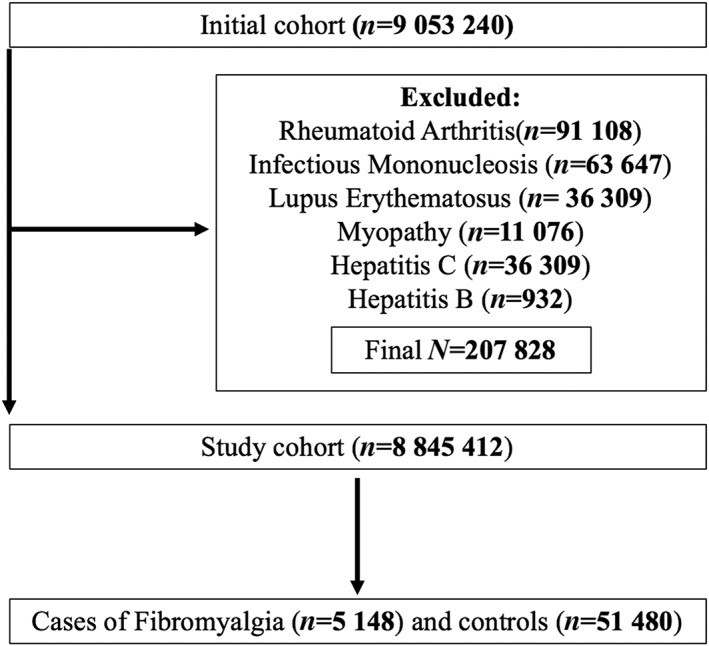
De la cohorte base, excluimos a aquellos con condiciones fuertemente correlacionadas con la fibromialgia y el uso de FQ, incluyendo hepatitis B y C, mononucleosis infecciosa, miopatías, artritis reumatoide y lupus eritematoso (Figura 1). Se incluyeron como casos a aquellos con el primer código ICD ‐ 9 o 10 de fibromialgia codificado por un reumatólogo. Los casos tuvieron que haber recibido al menos un código adicional después del primer código. La fecha del primer código se consideró la fecha índice. Se excluyeron los sujetos con códigos de fibromialgia previos que hubiera aplicado cualquier otro tipo de médico. Cada caso, se apareó con diez controles sin diagnóstico de fibromialgia a través de un muestreo basado en densidad, lo que aseguró que los casos estaban en riesgo de desarrollar fibromialgia y donde cada control podía convertirse en un caso futuro, generando odds ratios que se asemejan mucho a una relación de tasas en un estudio de cohorte [8]. Los casos se compararon con los controles por tiempo calendario, edad y sexo. Además, excluimos las condiciones que imitan la fibromialgia. Nos aseguramos de que los casos y los controles tuvieran al menos un año de datos para poder determinar el uso de los medicamentos incluidos en el estudio durante el año anterior a la fecha del evento.
Identificamos todas las recetas de FQ surtidas durante el año anterior a la fecha índice. Para controlar la latencia de la enfermedad y la causalidad inversa, no se tuvieron en cuenta los primeros 60 días antes de la fecha índice (días 0-60). La exposición se definió como el uso de al menos una receta de FQ en los días 61–365 previos a la fecha índice. Para controlar la posible confusión por infección viral o bacteriana, también examinamos el riesgo de fibromialgia con dos antibióticos diferentes, mutuamente excluyentes, amoxicilina y azitromicina, que no están químicamente relacionados con las FQ. Los que tomaron FQ no estuvieron expuestos a amoxicilina o azitromicina durante el período de exposición.
Se eligieron estos dos antibióticos porque tienen un mecanismo de acción diferente, ya que la amoxicilina se usa ampliamente en el tratamiento de infecciones bacterianas y la azitromicina generalmente se usa para infecciones respiratorias más graves, por su espectro más amplio de cobertura bacteriana y alta penetración en los tejidos. En el grupo de comparación constó de aquellos que no tomaron ninguno de los tres antibióticos incluidos en el estudio. La demografía entre casos y controles se evaluó mediante la prueba t de Student o la prueba de chi-cuadrado. La regresión logística condicional se utilizó para ajustar según el diagnóstico previo de hipotiroidismo, poliartritis reumática y enfermedad de Lyme.
Resultados
Identificamos 5.148 casos y 51.480 controles (Cuadro 1, ver en el enlace que aparece en el encabezado). Como la fibromialgia afecta principalmente a las mujeres, el 87% de los casos fueron mujeres. La razón de tasa ajustada (RR) para el uso de cualquier FQ, amoxicilina y azitromicina fueron 1,63 (IC 95%: 1,41–1,87), 1,64 (IC 95%: 1,46–1,85) y 1,68 (IC 95%: 1,49–1,89) (Cuadro 2, ver en el enlace del encabezado). Los RR para los pacientes que recibieron una o más de una receta fueron comparables entre los tres antibióticos (Cuadro 2). El RR para cualquier uso de FQ en comparación con cualquier uso de amoxicilina o azitromicina fue de 0,99 (IC del 95%: 0,83 a 1,18) y con la azitromicina fue de 0,97 (IC del 95%: 0,82 a 1,16).
Discusión
Los resultados de nuestro estudio indicaron que el riesgo de fibromialgia con FQ es similar al de la amoxicilina y la azitromicina. Estos datos indican que la posible asociación entre FQ y fibromialgia se podría deber a la infección viral o bacteriana para la que se prescriben. Una serie de estudios que han demostrado que la fibromialgia podría desencadenarse por un proceso infeccioso lo confirman [6]. Nuestros datos se corroboran por la inclusión de azitromicina, un antibiótico generalmente recetado para infecciones respiratorias más graves adquiridas en la comunidad. La azitromicina tiene una alta penetración en los tejidos y también se ha demostrado que afecta a las mitocondrias de los mamíferos [9] de forma similar a las FQ [10].
Se han postulado varios mecanismos para explicar el riesgo elevado de fibromialgia con los tres antibióticos. Primero, los estudios han demostrado que la fibromialgia puede desencadenarse por una respuesta inmune secundaria a un proceso infeccioso [6, 11]. Esto puede deberse a la activación del sistema inmune que lleva a un aumento de los niveles séricos de citocinas (IL-2, IL-8 y IL-2r) además de los linfocitos que expresan receptores opiáceos que responden a la sustancia P, un modulador primario del dolor [12]. Además, los estudios transversales han demostrado que el 20% de los pacientes con fibromialgia han informado una infección previa, y otro estudio informó que el 50% de los pacientes informaron “síntomas similares a la gripe” antes del diagnóstico de fibromialgia [6, 13]. En segundo lugar, se ha encontrado que las enfermedades que resultan de una microflora intestinal alterada, como el síndrome del intestino irritable, son muy frecuentes en pacientes con fibromialgia, alcanzando tasas tan altas como 81% [14, 15]. Un trabajo reciente también ha demostrado que los antibióticos alteran la microflora intestinal al eliminar las bacterias comensales y patógenas [16]. Por lo tanto, es posible que la disbiosis intestinal desempeñe un papel en el desarrollo de la fibromialgia. Si es cierto, la disbiosis de la microflora puede exacerbar aún más el estado inmunocomprometido de los pacientes con fibromialgia, ya que las bacterias comensales son críticas para mantener una respuesta inmune saludable [17].
La fortaleza de nuestro estudio es el gran tamaño de la muestra y que se ha manejado con mucho cuidado la latencia de la enfermedad y la causalidad inversa. Como con todos los estudios epidemiológicos y el uso de datos provenientes de facturas por servicios de salud, nuestro estudio tiene limitaciones. No tuvimos acceso a las historias clínicas de los pacientes. Tampoco tenemos información sobre antecedentes familiares de fibromialgia o consumo de alcohol, aunque es poco probable que estas variables, que son factores de riesgo y no factores de confusión, sesguen los resultados del estudio. Es posible que algunos de los casos que se han codificado como fibromialgia hayan sido una miopatía viral [18]. Sin embargo, este escenario es poco probable ya que generalmente los síntomas de infección viral se manifestarían en los primeros 60 días de usar una FQ, que es el período que excluimos del estudio.
En resumen, a pesar de los informes de caso en la literatura y los informados por varias agencias reguladoras de medicamentos de fibromialgia y uso de FQ, el riesgo parece ser similar al asociado con la amoxicilina y la azitromicina. Por lo tanto, puede deberse a una posible infección que desencadenó los síntomas de la fibromialgia.
Conflicto de interés
Los autores no declararon ningún conflicto de interés.
Referencias