| Registros de ensayos |
Registro prospectivo de ensayos |
| Registros actualizados |
| Publicación de los resultados en donde fueron registrados, en un plazo de 12 meses |
| Publicación del protocolo en donde fueron registrados, en un plazo de 12 meses |
| Publicación en revistas |
Publicación de los resultados en una revista |
| Número del ensayo incluido en todas las publicaciones |
| Publicación de acceso abierto |
| Control del cumplimiento |
El financiador supervisa el registro del ensayo |
| El financiador supervisa la notificación de resultados |
| El financiador publica los informes de seguimiento |
| Sanciones |
El financiador tiene en cuenta si el investigador principal ha publicado los informes antes de otorgar nuevas subvenciones. |
Norteamérica
La evaluación de TranspariMED puso de manifiesto la diversidad de resultados entre los financiadores estadounidenses.
Por ejemplo, los Institutos Nacionales de Salud de EE UU ya han adoptado 10 de las 11 salvaguardias de la OMS (y recientemente
empezaron a avanzar en los resultados pendientes), mientras que otros financiadores, como los Centros de Control de Enfermedades, parecen seguir repartiendo dinero público sin comprobar si los investigadores obtienen realmente los resultados prometidos [4].
Europa
En Europa continental, el panorama también es muy heterogéneo. Aunque ningún financiador europeo ha adoptado todas las salvaguardias recomendadas por la OMS, varios cuentan ahora con políticas sólidas, incluidos los financiadores públicos de Suecia, Noruega y Bélgica. Sin embargo, los financiadores públicos de Austria, Dinamarca, Alemania, Italia, Países Bajos y España siguen decepcionando.
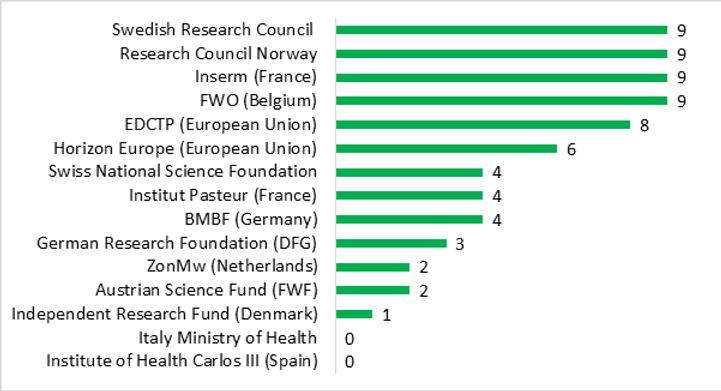 Nota: Varios de los financiadores que aparecen arriba reforzaron significativamente sus políticas durante 2021-2022. Para más información sobre las mejoras en cada financiador, ver este preprint [5].
Nota: Varios de los financiadores que aparecen arriba reforzaron significativamente sus políticas durante 2021-2022. Para más información sobre las mejoras en cada financiador, ver este preprint [5].
Reino Unido
El Instituto Nacional de Investigación en Salud del Reino Unido es el único financiador de alcance global que ha adoptado las 11 salvaguardias para evitar el desperdicio en la investigación, recomendadas por la OMS. El Medical Research Council, el otro gran financiador público del país, también obtuvo muy buenos resultados, al igual que el gigante filantrópico Wellcome Trust.
Oceanía y Asia Meridional
Los financiadores de estas regiones siguen teniendo grandes vacíos en sus salvaguardias para [evitar] el desperdicio en la investigación.
Sin embargo, parece probable que los financiadores de Oceanía mejoren pronto. El financiador de Nueva Zelanda completó recientemente una auditoría amplia de su cartera de ensayos, y el financiador de Australia está revisando la situación internamente [6].
Mapa de salvaguardias para los 39 financiadores
El siguiente gráfico muestra la adopción actual de las 11 salvaguardias recomendadas por la OMS para evitar el desperdicio en la investigación.
La OMS recomienda que todos los financiadores exijan que los resultados de los ensayos se hagan públicos en donde fueron registrados en el plazo de un año [7]. Sin embargo, hasta la fecha, sólo 18 de 39 financiadores han adoptado ese requisito. Diez financiadores ni siquiera exigen a sus beneficiarios que registren los ensayos antes iniciarlos, a pesar de que se trata de un requisito ético mundial de larga data.
Algo positivo es que una minoría significativa (y en rápido crecimiento) de financiadores ahora supervisaactivamente si los ensayos se registran e informan los resultados.
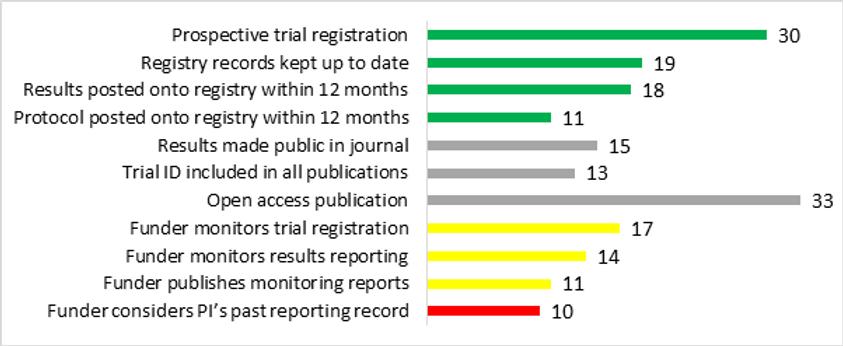 Nota: El código de colores del gráfico indica si la salvaguardia está relacionada con el registro (verde), las revistas (gris), la supervisión (amarillo) o las sanciones (rojo).
Nota: El código de colores del gráfico indica si la salvaguardia está relacionada con el registro (verde), las revistas (gris), la supervisión (amarillo) o las sanciones (rojo).
¿Qué pueden hacer los financiadores?
El informe de TranspariMED incluye una sencilla lista de comprobación y plantillas de texto que los financiadores pueden utilizar para reforzar sus políticas y sistemas.
El reporte se puede descargar en la página web que se señala en el encabezado. Además, los 39 financiadores estudiados pueden ahondar en la información recopilada para cada uno accediendo a los estudios de apoyo, también disponibles en dicha página.
¿Y ahora qué?
TranspariMED volverá a evaluar a los 39 financiadores a principios de 2024 para hacer un seguimiento de sus avances.TranspariMED agradece el apoyo financiero de la comunidad para continuar con sus investigaciones. TranspariMED no acepta financiación de la industria
Muchas gracias a nuestros voluntarios
La evaluación de 2023 fue gestionada de principio a fin por dos increíbles becarias de TranspariMED, Elise Gamertsfelder (financiadores estadounidenses[8]) y Marguerite O’Riordan (todos los demás financiadores[5]).
En su trabajo contaron con el apoyo de los siguientes voluntarios:
- Netzahualpilli Delgado Figueroa
- Sarai Keestra
- Alan Rossi Silva
- Ronak Borana
- Max Siebert
- Martin Haslberger
- Carolina Cruz
- Tarik Suljic
Nota de Salud y Fármacos. Ed Silverman publicó un artículo en el que difundía esta investigación [9]. A continuación, se encuentra la selección de información adicional.
Con respecto a EE UU, la nota de prensa comenta que sólo el 37% de las 14 mayores organizaciones públicas y filantrópicas que financian la investigación clínica en EE UU han aplicado las mejores prácticas de divulgación recomendadas por la OMS. Un aspecto positivo y común a todas las organizaciones es que las 14 exigen la publicación sea de acceso abierto. No obstante, medidas tales como exigir el registro previo del ensayo, la publicación de resultados en un sitio web, la publicación de resultados en revistas, la identificación de los ensayos en la publicación y la publicación de informes de seguimiento por parte de los financiadores, no se aplican de forma generalizada.
De manera específica, el artículo comenta que, según un informe publicado el 2022 por la Oficina del Inspector General del Departamento de Salud y Servicios Humanos, “Los NIH no verificaron que los resultados de la mitad de los 72 ensayos financiados se informaran en 2019 y 2020 a ClinicalTrials.gov”. No obstante, según la investigación de TranspariMED, en promedio las instituciones públicas de EE UU adoptaron más las recomendaciones de la OMS (48%) que los financiadores filantrópicos del mismo país (25%).
El informe de Transparimed incluye información detallada sobre la adherencia a los principios de transparencia de la OMS por parte de las agencias gubernamentales estadounidenses y también sobre las organizaciones filantrópicas.
Referencias
- Bruckner, T. NIH waste far over $100 million in medical research funding every year – new study. TranspariMED, 21 de febrero [2023]. https://www.transparimed.org/single-post/nih-research-waste
- Bruckner, T. Clinical trial transparency – A guide for policy makers. Cochrane, The Collaboration for Research Integrity and Transparency (CRIT), The Pharmaceuticals & Healthcare Programme (PHP) of Transparency International (TI) y TranspariMED, diciembre de 2017. https://docs.wixstatic.com/ugd/01f35d_def0082121a648529220e1d56df4b50a.pdf
- OMS. Joint statement on public disclosure of results from clinical trials. 18 de mayo de 2017. https://www.who.int/news/item/18-05-2017-joint-statement-on-registration
- Bruckner, T. NIH crack down: report your clinical trial results or face sanctions. TranspariMED, 26 de marzo [2023]. https://www.transparimed.org/single-post/nih-clinical-trials-compliance
- O’Riordan, M., Haslberger, M., Cruz, C., et al. Are European clinical trial funders policies on clinical trial registration and reporting improving? – A cross-sectional study. [Preprint]. MedRxiv, 6 de abril de 2023. https://www.medrxiv.org/content/10.1101/2023.04.05.23288169v1.full.pdf
- Bruckner, T. New Zealand: Clinical trials audit finds high reporting rates but slow reporting speeds. TranspariMED, 24 de octubre de 2022. https://www.transparimed.org/single-post/new-zealand-clinical-trials-audit-finds-high-reporting-rates-but-slow-reporting-speeds
- Bruckner, T. Why is uploading clinical trial results onto trial registries so important? TranspariMED, 27 de enero de 2020. https://www.transparimed.org/single-post/2019/04/24/why-is-uploading-clinical-results-onto-trial-registries-so-important
- Gamertsfelder, E., Delgado-Figueroa, N., Keestra, S., et al. Adoption of the World Health Organization’s best practices in clinical trial registration and reporting among top public and philanthropic funders of medical research in the United States. [Preprint]. MedRxiv, 3 de abril de 2023. https://www.medrxiv.org/content/10.1101/2023.04.03.23288059v1
- Silverman, E. Most large U.S. funders of clinical research have poor transparency policies, analysis finds. Statnews, 17 de abril de 2023. https://www.statnews.com/pharmalot/2023/04/17/transparency-clinical-trials-nih-cdc-gates/
creado el 31 de Agosto de 2023