Informe revela que Chile es el país que más ensayos clínicos realiza en Latinoamérica y muestra que actualmente se están desarrollando 408 ensayos clínicos y que entre 2012 y 2023 se aprobaron 1.107 de estas pruebas médicas en el país.
Aunque no existen estudios sobre la experiencia de participantes en este tipo de pruebas, según el Estudio de Opinión sobre los Ensayos Clínicos en Chile, elaborado por el Centro Basal IMPACT de la Universidad de los Andes, un 28% de los chilenos admite que participaría de estos ensayos, porcentaje que aumenta casi el doble si el voluntario dispusiera de información completa sobre el tema.
Un 89% de los encuestados cree que es muy importante y extremadamente importante la realización de estas pruebas, y a medida que aumenta la edad de quienes participaron en el sondeo, sube el porcentaje que opina que son muy importantes.
Informe revela que Chile es el país que más ensayos clínicos realiza en Latinoamérica
Para fortalecer la ejecución de estas pruebas, la Cámara de la Innovación Farmacéutica (CIF), que agrupa a los principales laboratorios y fabricantes de fármacos que operan en el país, creó la Mesa de Colaboración para la Investigación Clínica en Chile, instancia que involucra a diversos actores para impulsar políticas que faciliten y aumenten los ensayos clínicos en el país.
Ahora, un informe de esta Mesa indica que hay 123 países con al menos un ensayo clínico en ejecución financiado por la industria, una lista que encabeza Estados Unidos, seguido por China, España, Francia y Reino Unido.
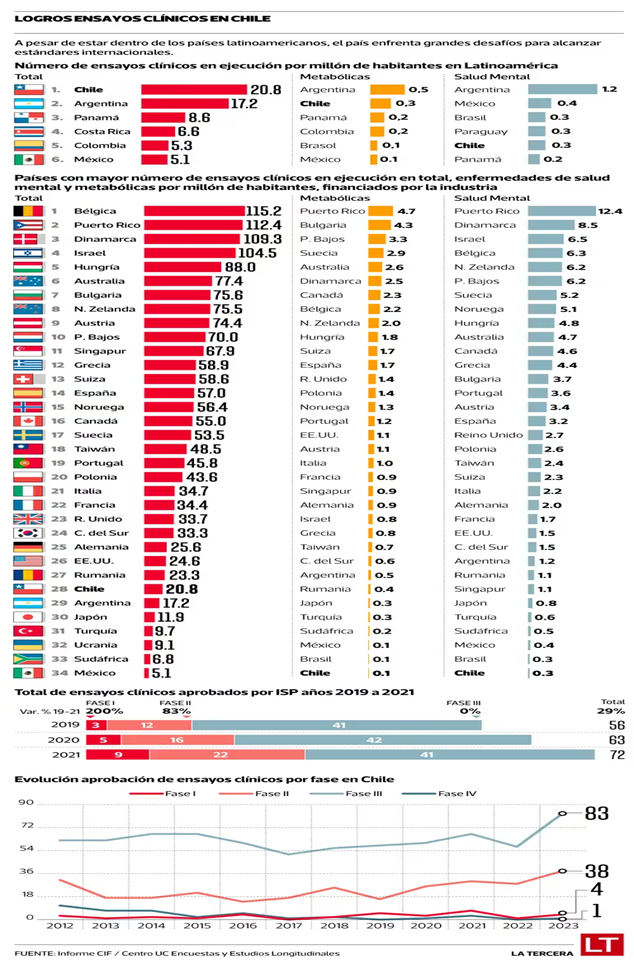
Chile se encuentra en el puesto 31, con 408 ensayos clínicos en marcha hasta mayo de 2023. De acuerdo al informe, el país registra 20,8 estudios por millón de habitantes, liderando la realización de estos ensayos per cápita en Latinoamérica, los que demandaron una inversión de US$ 122 millones en 2021.
Chile es el país que más ensayos clínicos realiza en la región
De acuerdo al documento, este liderazgo fue especialmente valioso durante la pandemia. En 2020, el Covid-19 llevó a Chile a crear leyes especiales que flexibilizaron las restricciones de la Ley Ricarte Soto para tratamientos contra el coronavirus, convirtiendo a Chile en el país con más ensayos clínicos del Sars-CoV-2 en la región, dándole una ventaja significativa en el manejo de la pandemia.
Sin embargo, pese a estas ventajas, Francisca Rodríguez, gerenta de Innovación y Salud de la CIF, dice que el país enfrenta desafíos para competir a nivel internacional. “El principal desafío son las barreras regulatorias de la Ley Ricarte Soto”, señala.
Esto, asegura, ya que la ley obliga al patrocinador a proporcionar tratamiento post ensayo indefinidamente y asumir responsabilidad a priori por cualquier daño futuro. Esto aumenta los costos de seguros y encarece las investigaciones. Además, dice Rodríguez, se necesita una política estatal que fomente estos ensayos mediante la difusión, aceleración de procesos y generación de incentivos para la participación de hospitales.
Para agilizar la aprobación de ensayos clínicos en Chile, señala la gerenta, se necesitan más profesionales y mejor tecnología en el ISP y comités de ética. También, es crucial permitir revisiones simultáneas por el Comité de Ética y el ISP, manteniendo una comunicación fluida entre ambos, explica Rodríguez.
Crecimiento de ensayos clínicos en Chile
Para abordar la falta de datos específicos sobre la inversión en ensayos clínicos en Chile, la CIF, junto con InvestChile y la Universidad Católica realizó una encuesta entre las compañías socias de la CIF, que representan el 90% de la innovación farmacéutica en el país.
Los datos muestran que entre 2012 y 2023, se aprobaron 1.107 ensayos clínicos en Chile, de los cuales el 95% fueron financiados por la industria farmacéutica. El año 2023 fue notable, con 127 estudios aprobados por el ISP, lo que representa un incremento promedio del 13,5% anual desde 2012. Además, entre 2019 y 2021, se observó un crecimiento del 29% en el número total de ensayos, alcanzando 72 estudios en ese periodo.
Estos ensayos incluyen medicamentos, dispositivos, suplementos alimenticios, radioterapia y tratamientos conductuales. A nivel mundial, el 57% de estos estudios son financiados por universidades, hospitales u organizaciones relacionadas, mientras que el 36% son financiados por la industria farmacéutica.
Asimismo, la encuesta mostró que, los laboratorios farmacéuticos en Chile valoran positivamente la infraestructura física, la capacidad de recursos humanos, las condiciones epidemiológicas y geográficas para realizar ensayos clínicos en el país. Sin embargo, existen opiniones mixtas sobre las condiciones regulatorias, la coordinación entre instituciones, la certidumbre de los costos asociados y el tamaño de la población. Las peores evaluaciones se dan en el tiempo de aprobación de los comités de ética y la adopción de medicamentos por el sistema de salud.
Otros desafíos incluyen los requerimientos post estudios, el conocimiento general de los estudios y el elevado costo comparado con otros países de la región, lo que reduce la competitividad de Chile para la inversión en ensayos clínicos.
Mayor inversión y publicidad
Diferentes países han implementado políticas para atraer ensayos clínicos, mejorando su posición en términos de estudios e inversión en I+D. Australia se ha destacado en ensayos de fase I y España aumentó su inversión de 479 millones de euros en 2012 a 834 millones en 2022. Estos avances fueron logrados mediante la colaboración entre diversos actores y la implementación de acciones para agilizar procesos, aumentar la difusión y homologar regulaciones.
Por lo que es importante que el país pueda aprender lecciones de otros países como Australia y España, de donde se puede mirar la importancia de un mandato gubernamental claro para fortalecer el ecosistema de investigación clínica. Este fortalecimiento se logra a través de la colaboración público-privada, involucrando a todos los actores del sector.
“La clave está en combinar un marco regulatorio eficiente, incentivos económicos, promoción, una infraestructura de investigación robusta, y un enfoque en la colaboración y capacitación” añade Rodríguez.
El Dr. Christian Caglevic, director Científico Departamento de Investigación del Cáncer y Jefe Unidad de Estudios Clínicos de la FALP, quien participó del informe CIF, añade que en otros países como Estados Unidos y Europa, existen estrategias efectivas de difusión de ensayos clínicos que pueden ayudar también a fortalecer este rubro en el país.
Esto incluye publicidad en televisión, revistas, y páginas web especializadas en centros médicos y oncología. Además, personalidades públicas y celebridades comparten sus experiencias y animan a la participación en este tipo de pruebas.
Implementar estas estrategias en Chile podría aumentar la conciencia pública y la participación en estudios clínicos, “porque ellos saben que a veces la mejor opción para un paciente es participar de un ensayo” comenta Caglevic.
El estudio UC también muestra que la industria farmacéutica de innovación invirtió US$122 millones de dólares en 2021 en Chile, lo que se estima equivale al 10,7% del gasto en I+D a nivel nacional y 26% del gasto del sector empresas.
Aunque ha subido la inversión, el informe hace hincapié en que el país tiene la capacidad de crecer dos o tres veces, por lo que dejar de recibir ensayos o no aumentar su número, incide en brechas de conocimiento científico, inversión en I+D, desarrollo de capacidades, de infraestructuras, etc.
Según Rodríguez, además de mitigar el impacto negativo de la Ley Ricarte Soto, dice que es necesario revisar y alinear la legislación con las normativas internacionales. Esto incluye retomar la discusión del proyecto de ley sobre regulación de ensayos clínicos de productos farmacéuticos (boletín Nº 13.829-11) para hacer a Chile más competitivo en la atracción de estas pruebas y diversificar las áreas terapéuticas investigadas.
“Adicional y posterior al cambio legal, es necesario elaborar una regulación más clara, definida y específica para ensayos clínicos, donde se promueva la ejecución en sus diferentes fases y se aborde el proceso de ejecución, condiciones y responsabilidad de los diferentes actores”, añade Rodríguez.
¿Cómo funcionan los ensayos clínicos en Chile?
En Chile, según la normativa de buenas prácticas clínicas, sólo se puede participar de ensayos clínicos siendo voluntario. No obstante, las instituciones patrocinadoras de los ensayos podrán compensar los gastos de traslado y cubrir los costos de exámenes relacionados con la participación del estudio.
Para que un paciente participe de un ensayo clínico, debe firmar un consentimiento informado, en el que se le explica detalladamente acerca del tratamiento, procedimientos, el tiempo de participación y el resguardo de la información personal. Durante la ejecución del estudio se evalúan posibles contraindicaciones que resguarden la seguridad del paciente.
Los ensayos clínicos son estudios en personas voluntarias para evaluar la eficacia y seguridad de métodos diagnósticos, medicamentos, vacunas y otras intervenciones. Estos estudios pueden durar entre 10 y 15 años, con menos del 1% de los descubrimientos obteniendo aprobación regulatoria. [Nota de SyF: en realidad la tasa de moléculas que se testan en humanos y acaban siendo aprobadas por las agencias reguladoras es de alrededor del 10%, dependiendo de la especialidad clínica – pero las que son más efectivas y seguras que los tratamientos existentes son muy pocas).
Un estudio clínico comienza cuando una empresa, universidad o investigador busca probar un producto para su comercialización. El patrocinador del estudio asume responsabilidades legales y financieras, pero puede delegar tareas como la solicitud de autorización al ISP, la aprobación de comités de ética y la gestión del estudio.
Una vez aprobados, el estudio se ejecuta en establecimientos de salud y se considera activo desde el reclutamiento del primer paciente hasta la última visita del último paciente reclutado.