ENSAYOS CLÍNICOS
Regulación, registro y diseminación de resultados
Medicamentos nuevos: transparencia
(New drugs: transparency)
Aust Prescr 2014;37:27
http://www.australianprescriber.com/magazine/37/1/artid/1488
Traducido y resumido por Salud y Fármacos
Australian Prescriber necesita tener acceso a la información que se obtiene durante la realización de los ensayos clínicos para poder hacer comentarios sobre los medicamentos nuevos en la revista. La agencia reguladora de Australia (Therapeutic Goods Administration –TGA) utiliza mucha información que no se publica cuando evalúa los medicamentos nuevos. Australian Prescriber solicita rutinariamente a las compañías farmacéuticas una copia de la evaluación clínica en la que se sustenta la información de seguridad y eficacia de sus productos. Pocas compañías responden con este nivel de transparencia.
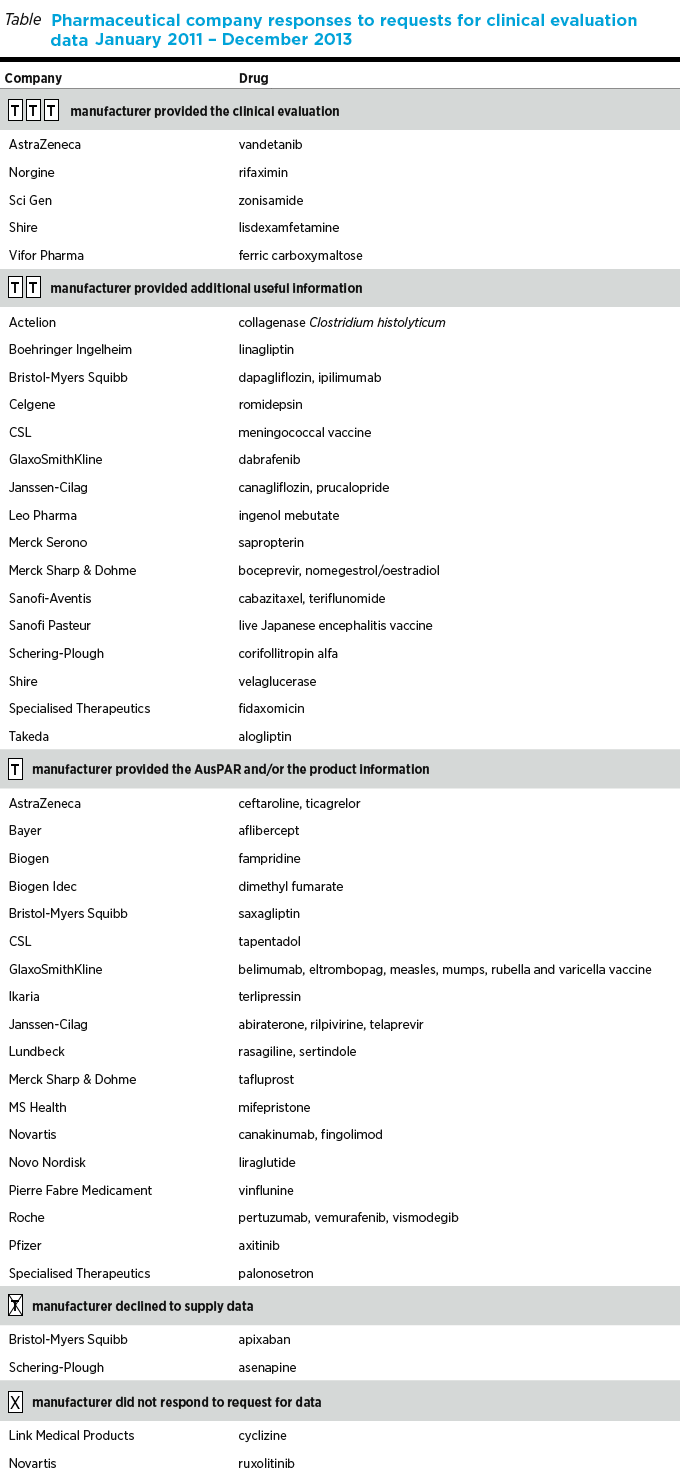
Australian Prescriber empezó a publicar el nivel de cooperación de las compañías hace casi 10 años. Para esto utilizamos la clasificación T. Mientras algunas compañías proveen la información, otras ni siquiera responden a nuestra solicitud de información (Ver Cuadro).
Durante los últimos años, TGA ha empezado a publicar información sobre los elementos que se tuvieron en cuenta al evaluar un producto nuevo para el mercado australiano. Estas evaluaciones públicas (Australian Public Asssessment Reports –AusPARs) incluyen información de la evaluación clínica realizada por TGA. Esto ha significado que algunas compañías, al recibir la solicitud de Australian Prescriber en lugar de proporcionarnos la información nos refieran a AusPAR. Como el documento AusPAR es de dominio público y no incluye la totalidad de la evaluación clínica, el comité ejecutivo de editores decidió que las compañías que solo nos dieron acceso a AusPAR, recibirían la calificación más baja de la puntuación T.
Leer los AusPAR es especialmente importante cuando todavía no se han puesto a disposición del público y el producto nuevo ya está disponible en el mercado australiano. La TGA está intentando reducir este atraso en la publicación de los AusPARs. Además, en julio de 2013, la TGA ha anexado resúmenes de sus propias evaluaciones a los AusPARs.
La transparencia en la regulación de los medicamentos mejora gradualmente, pero Australian Prescriber seguirá publicando la disposición de la industria farmacéutica para compartir la información de los ensayos clínicos de medicamentos nuevos