Todos los Tratados de Libre Comercio (TLC) de EE UU que se han firmado en los últimos 20 años han exigido que los socios comerciales promulguen leyes de propiedad intelectual (PI) más estrictas que las requeridas en el acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (ADPIC) de la Organización Mundial del Comercio.
En los mercados farmacéuticos, estas reglas que se conocen con el nombre de “ADPIC-Plus”, incrementan el poder de monopolio de los productores de medicamentos de marca, extendiendo su período de exclusividad en el mercado al excluir la competencia de los genéricos. No obstante, los estudios que miden el impacto de determinados TLCs sobre los precios de los medicamentos, a menudo han detectado efectos pequeños, ya que tardan mucho en hacerse completamente evidentes. En cambio, los estudios que han estudiado el efecto de las normas ADPIC-Plus en otras variables como: las extensiones de plazo de patentes o las leyes sobre la protección de datos de prueba, con frecuencia han detectado impactos significativos en los precios o en la disponibilidad de medicamentos. Sin embargo, muchos de los estudios existentes se han centrado en un solo país y/o en unos pocos medicamentos.
En este documento de trabajo, utilizo otro acercamiento y me centro en una disposición de los ADPIC-plus que exigen todos los TLCs estadounidenses, y demostraré que se ha asociado con un incremento más rápido de los precios de los productos farmacéuticos que importaron los 42 países que firmaron estos TLCs. Específicamente, la investigación muestra que el precio de los medicamentos importados aumentó, en promedio, entre 2,4 y 4,5 puntos porcentuales más rápidamente en los países que implementaron la exclusividad de datos que en los que no lo hicieron.
La exclusividad de datos es una forma de protección de la propiedad intelectual que se aplica al uso de los datos de los ensayos clínicos. Cuando una empresa innovadora lanza un nuevo medicamento, debe presentar los datos de los ensayos clínicos a las agencias reguladoras para demostrar que el producto es seguro y eficaz. Cuando los fabricantes de genéricos solicitan el permiso de comercialización, generalmente se basan en los datos de los ensayos clínicos presentados por la compañía innovadora, lo que les permite sacar productos al mercado sin repetir los ensayos clínicos, algo que posteriormente se traduce en precios al consumidor más bajos.
La exclusividad de los datos abarca cierto período de tiempo, generalmente entre 5 y 12 años, durante el cual las compañías de genéricos no pueden obtener el permiso de comercialización para sus productos basándose en los datos clínicos presentados por las empresas innovadoras, bloqueando así el ingreso de sus productos al mercado. Es un tipo de protección de la PI diferente del derecho de patente, que puede bloquear la competencia de genéricos después de que expire la patente.
El documento de trabajo utiliza un estudio de 2011 de la Federación Internacional de Asociaciones y Fabricantes de Productos Farmacéuticos (IFPMA) que identificó las leyes que rigen los datos de los ensayos clínicos en 41 países. De estos, el Banco Mundial califica a 16 como países de altos ingresos y al resto como países de medianos ingresos. El conjunto no incluye ningún país de África subsahariana, pero sí incluye países de América, Europa, Asia y África del Norte.
La Figura 1 muestra cómo aumentó la protección de la exclusividad de datos en este conjunto de países a lo largo del tiempo. Hong Kong ha tenido exclusividad de datos de facto desde que estableció su regulación de productos farmacéuticos y venenos (“Pharmacy and Poisons Regulations”) en 1970, que exigía que todos los solicitantes presentaran datos clínicos (desde entonces se ha revisado para permitir solicitudes abreviadas para los productos genéricos después de un período de exclusividad de datos). EE UU implementó tempranamente la exclusividad de datos, cuando se aprobó la Ley Hatch-Waxman en 1984. Inicialmente, había pocos países que protegieran los datos de prueba; solo otros cuatro países del conjunto analizado promulgaron la exclusividad de datos antes de 2000. Muchos otros países adoptaron la exclusividad de datos en la década de 2000. En total, 33 de los 42 países del conjunto incluyeron la exclusividad de datos en sus legislaciones antes de la publicación del informe IFPMA.
Figura 1: Cronograma de la implementación de la exclusividad de datos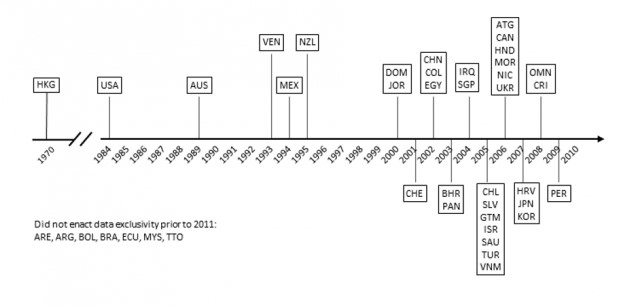
Fuente: Palmedo, 2021
Algunos países, como Chile, Guatemala y Jordania, introdujeron la exclusividad de datos a partir de la firma de TLC con EE UU, que los obligaba a hacerlo, pero ese no sucedió con todos.
La base de datos Comtrade de la ONU muestra lo que sucedió con el precio de las importaciones cuando estos países implementaron la exclusividad de datos. Comtrade informa el valor anual (en dólares estadounidenses) y el volumen (en kilogramos) de las importaciones farmacéuticas comerciales según lo registrado por las autoridades fronterizas. A diferencia de los precios publicados, que pueden estar sujetos a más descuentos o aumentos, Comtrade informa las cantidades reales que se han pagado al por mayor. Desde mediados de la década de 1990 hasta el presente hay datos disponibles sobre las importaciones anuales en muchos países y están agregados por clase de producto.
La Figura 2 compara el precio promedio anual por kilogramo importado para cada país según hayan o no adoptado la exclusividad de datos entre 1996 y 2010. Se muestra que el precio aumentó a una tasa mayor en los países que promulgaron la exclusividad de datos. Los precios promedio en cada grupo tendieron a ser similares hasta principios de la década de los 2000s, y comenzaron a divergir después del 2004, a medida que más países implementaron la exclusividad de datos en sus legislaciones locales.
Figura 2: Precio promedio por kilogramo de importaciones farmacéuticas (USD)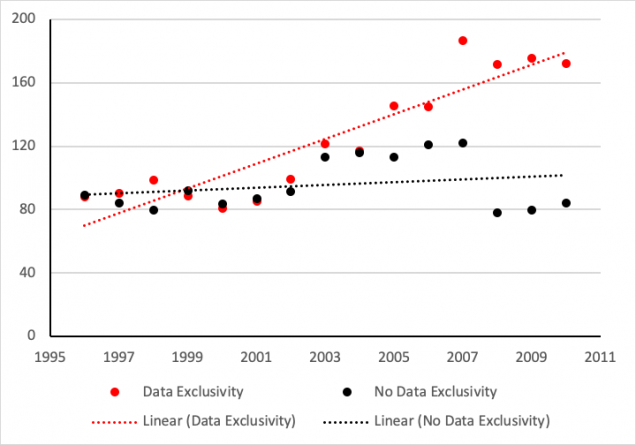
Fuente: Palmedo, 2021
La relación entre la exclusividad de datos y un mayor aumento en el precio en las importaciones farmacéuticas es estadísticamente significativa y robusta cuando se incluye un comparador En este conjunto de países se hicieron pruebas econométricas, ajustando por la riqueza del país, el volumen de las compras anuales, los niveles del gasto en salud y el monto del gasto de bolsillo. Pruebas que miden con mayor precisión el nivel de asociación entre las variables, confirmaron los hallazgos originales. En general, la tasa promedio de crecimiento anual de los precios después de que los países implementaron la exclusividad de datos fue de 2,4 a 4,5 puntos porcentuales.
Estos resultados vinculan la política comercial estadounidense con precios más altos de medicamentos en el extranjero. Todos los tratdos de libre comercio más recientes de EE UU requieren que las contrapartes promulguen la exclusividad de los datos, incluyendo aquellos firmados con países de medianos y bajos ingresos, donde las personas y los sistemas de salud no pueden afrontar precios más elevados.
EE UU pronto comenzará las negociaciones del tratado de libre comercio con Kenia, un país con un PIB per cápita de US$1.856. Es evidente que Kenia no tiene interés en pagar más por los medicamentos que importa, pero los grupos de la industria estadounidense están abogando por incluir normas que exijan una protección más estricta de los datos de pruebas y patentes en ese país. Al mismo tiempo, la pandemia de covid-19 ha llamado la atención sobre las desigualdades en el acceso a vacunas, medicamentos y otras tecnologías sanitarias esenciales. Es hora de corregir la política comercial de EE UU, para que deje de promocionar las reglas de propiedad intelectual ADPIC-Plus, que empeoran esta desigualdad global.
Se puede leer el informe completo (en inglés) en este enlace: https://www.bu.edu/gdp/2021/04/21/evaluating-the-impact-of-data-exclusivity-on-the-price-per-kilogram-of-pharmaceutical-imports/