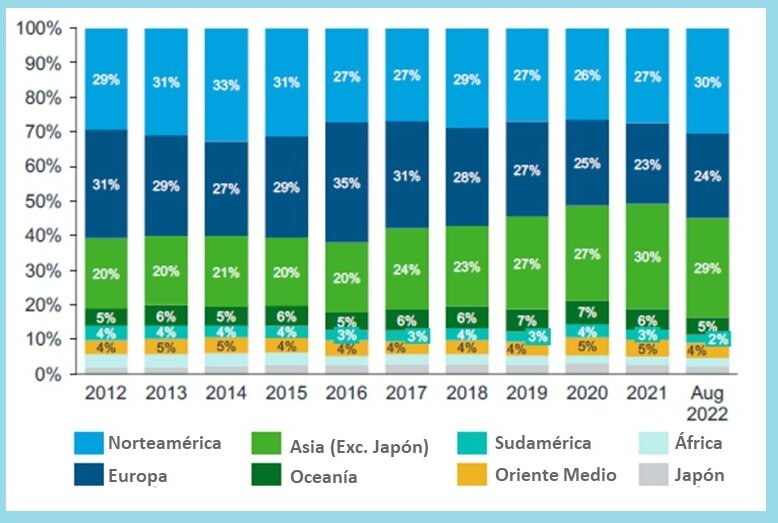
Europa ha pasado de realizar un 31% de los ensayos en el mundo en 2012 a un 24% en 2022, frente al 29% de Asia, que partía de un 20%.
Si bien España es líder en ensayos clínicos en Europa contra la covid (https://www.diariomedico.com/medicina/empresas/espana-lider-europeo-en-ensayos-clinicos-frente-la-covid-19.html), con 1.200 millones de euros anuales invertidos en I+D, y solo cuarto en el mundo (https://www.farmaindustria.es/web/otra-noticia/espana-cuarto-pais-del-mundo-y-primero-de-europa-en-ensayos-clinicos-de-tratamientos-contra-el-coronavirus/) – tras China, Estados Unidos e Irán-, Europa está perdiendo terreno frente a las economías emergentes de Asia en los últimos 10 años.
Tanto es así que nuestro continente ha pasado de realizar en 2012 un 31% de los ensayos en el mundo a un 24% en 2022 (de enero a agosto). Por el contrario, Asia ha pasado de un 20% a un 29%, mientras Estados Unidos se ha mantenido constante (de un 29% a un 30%).
Así lo ha explicado Icíar Sanz de Madrid, directora del departamento Internacional de Farmaindustria, en el XVIII Seminario Industria Farmacéutica & Medios de Comunicación, organizado por la patronal de la industria farmacéutica innovadora: “Esto es una señal o un indicativo más de que la industria farmacéutica en Europa no goza de buena salud, no está en plena forma, porque su participación en ensayos a nivel mundial está descendiendo”.
En el mismo sentido, Sanz de Madrid se ha referido también a cómo ha perdido terreno en nuevos medicamentos aprobados: “Hace 30 años el 43% de los medicamentos aprobados se originaban en Europa y en Estados Unidos el 21%; ahora, en los últimos cinco años hasta 2021, se han invertido las cifras, con un 52% de las innovaciones producidas en Estados Unidos”.
Y ha aportado otro indicador: en 2020-21 los fondos de capital riesgo invirtieron en terapia génica en Estados Unidos un total de 16.000 millones de euros frente a los 3.000 millones de euros de Europa. “Algo estamos haciendo mal en Europa cuando en el pasado no ocurría esto”, ha añadido.
Ya lo avisaban investigadores de Arabia Saudí, Australia y Reino Unido en un artículo publicado en 2019: Clinical trials in Asia: A World Health Organization database study. Entre 2008 y 2017 los ensayos clínicos realizados en Asia se multiplicaron por siete, con un incremento mayor que en países como Estados Unidos.
Según este artículo, los países asiáticos que más destacaron fueron Japón, con un 30,8%, e Irán, con un 41,9%. En este último el número de ensayos pediátricos se incrementó de manera anual más que en ningún otro, a un ritmo de 30,4%.
A juicio de estos investigadores, este cambio podría atribuirse, entre otras cosas, a la mayor capacidad de estos países para reclutar pacientes naive. De hecho, afirman que en EEUU y Europa aproximadamente el 35% de los retrasos en los ensayos se deben al reclutamiento de pacientes, y una quinta parte de los ensayos en estos países no reclutan un número suficiente de sujetos. Añaden que, no en vano, Asia es el continente más poblado del mundo, con más de la mitad de la población mundial.
Además, otro factor es el coste de los ensayos clínicos: en Asia es entre un 30% y un 40% más bajo que en EEUU y la Unión Europea: “El coste combinado de cada paciente por visita en China, India y Tailandia equivalen al coste por paciente por visita solo en EEUU”. Añaden como causas la proliferación de organizaciones de investigación por contrato y un mejor entorno regulatorio.
Ante esta situación, ¿qué propone Farmaindustria? Mejorar el sistema regulatorio, “que es muy poco competitivo, muy lento, que no es capaz de responder sin demoras a las nuevas necesidades”; apostar por la innovación a través de un régimen de incentivos de primer nivel (de propiedad industrial y regulatorios) y mejorar el acceso con políticas adecuadas.
Sin embargo, en relación con los incentivos, Sanz de Madrid ha explicado que la Unión Europea propone algo “precocupante”: bajarlos y condicionarlos a la obligación de comercializar en todos los estados miembro de la Unión Europea: “Así no vamos a provocar una mejora en el acceso. Tendremos que dialogar con la UE y los estados miembro”, ha asegurado.
Más medicamentos huérfanos en Europa
Pese a estos malos augurios, también hay buenas noticias. Así, solo en 2021 Europa inició en 2021 en torno a 6.835 ensayos clínicos en diversas áreas terapéuticas, centrados en cinco áreas (Oncología, Infecciosas, Neurología, Hematología y Respiratorio). De estos, unos 1.800 (30%) han sido en medicamentos huérfanos. “Esto es una buena noticia, porque hay un 95% de enfermedades que aún no tienen solución terapéutica”.
Sanz de Madrid también asegura que hay más nuevos principios activos (API) aprobados por la Agencia Europea del Medicamento (EMA) en 2021 que de nuevas indicaciones: 59% frente a 41%. De hecho, el número de nuevos API aprobados en 2021 fue un 28% superior que el año anterior.
Por su parte, Emili Esteve, director técnico de Farmaindustria, ha llamado a ser “entusiastas del medicamento, porque eso significa que lo valoramos. Durante la covid aquí se ha seguido trabajando y haciendo investigación, de covid y fuera del covid”. De hecho, ha destacado que la industria farmacéutica española fabricó en 2021 un total de 12.100 millones de dosis de vacunas.
Es decir, ha puesto el acento en el “potente tejido industrial de nuestro país”, que cuenta con 173 plantas productivas repartidas por toda España: 103 plantas de medicamentos de uso humano (11 de ellas de medicamentos biológicos), 46 plantas de principios activos y 24 plantas de medicamentos veterinarios.
Citrasacurio y midazolam, en Cataluña
“La industria de principios activos ha sido también muy importante”. Y ha puesto dos ejemplos: “En la época del covid estaba el citrasacurio, que se fabricaba en Cataluña. Y cuando no había producto, porque había muchos pacientes en las UCIS, como teníamos una planta en Barcelona, pudimos suministrarlo”, ha detallado.
Igual sucedió con el midazolam, “que se fabricaba también en Cataluña. Lo tuvimos para la semana siguiente a cuando me reuní, un domingo de Pascua, con el resto de agentes, como la Aemps. Si hubiéramos tenido que pedirlo, probablemente no lo hubiéramos tenido”.
Esteve ha destacado que “tenemos un producto estratégico, un sector que hace esos puentes, con plantas de principios activos y de medicamentos veterinarios que no debemos denostar, porque nos han permitido convertir unas en otras en un momento determinado de necesidad”. Sí que ha expresado su deseo de tener más plantas biotecnológicas, “pero el incremento es creciente. Y es una oportunidad”.
Nota de Salud y Fármacos: Teniendo en cuenta que solo el 10% de las moléculas que se testan en humanos son aprobadas por las agencias reguladoras, y de que solo entre el 8 y el 10% de las moléculas que se aprueban son mejores que otros tratamientos existentes, Salud y Fármacos ve con beneplácito esa disminución de los ensayos clínicos en Europa y desearía que se extendiera a otros países hasta que los patrocinadores sean más cuidadosos con los diseños y la experimentación en humanos sea más eficiente. Salud y Fármacos considera que los ensayos clínicos financiados por la industria no contribuyen a desarrollar científicos ni representa una fuente de ingresos significativa para los países.