Expertos en vacunas de gran prestigio han publicado una editorial en el Stanley New England Journal of Medicine [1], en la que reconocen que no se invierte lo suficiente en monitorear la seguridad de las vacunas y que resumimos a continuación.
Según la editorial, los ensayos de Fase 3 no pueden detectar los eventos adversos poco frecuentes, por lo que cuando se aprueban las vacunas hay que establecer mecanismos de vigilancia para detectar señales de seguridad; y hay que hacer estudios para ver si hay una relación causal entre los efectos adversos y las vacunas. Estos estudios podrían ayudar a desarrollar vacunas más seguras, determinar las contraindicaciones de la vacunación y la compensación que debe recibir los que experimenten un evento adverso relacionado con la vacuna.
La editorial añade que el progreso en la ciencia de la seguridad de las vacunas haya sido lento (a menudo, en función de pruebas epidemiológicas que se retrasan o son inadecuadas para sustentar conclusiones causales y no permiten entender completamente los mecanismos biológicos). Mencionan que aunque se hicieron más de una docena de estudios epidemiológicos que llevaron a concluir que las vacunas contra el sarampión, las paperas y la rubéola y el timerosal en las vacunas no causaban autismo, los resultados no estuvieron disponibles hasta años después de que se cuestionara esa posibilidad. La lentitud de la ciencia contribuyó a la preocupación pública generalizada y a las consiguientes disminuciones en la cobertura de inmunización, así como a los brotes de sarampión.
En 234 revisiones de diversas vacunas y resultados de salud realizadas entre 1991 y 2012, el Instituo de Medicina (IOM) encontró pruebas inadecuadas para probar o refutar la causalidad en 179 (76%) de las relaciones que se estudiaron. En 2024, las Academias Nacionales de Ciencias, Ingeniería y Medicina emitieron un informe sobre los posibles daños de las vacunas contra la COVID-19 y no pudieron encontrar evidencia suficiente de una relación causal para 65 conclusiones (76%) (solo hubo evidencia suficiente en 20 conclusiones).
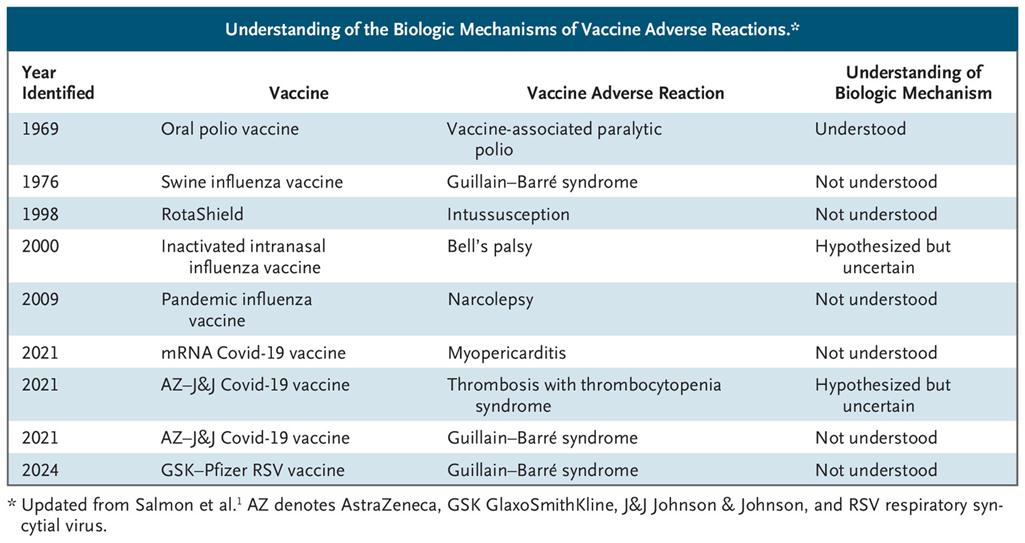
El mecanismo biológico sigue sin esclarecerse en el caso de la mayoría de las reacciones adversas a las vacunas, en particular, el síndrome de Guillain-Barré después de la administración de la vacuna contra la influenza de 1976-1977 y varias otras vacunas posteriores, la miocarditis después de las vacunas contra la COVID-19 basadas en ARNm y la invaginación intestinal después de la primera vacuna contra el rotavirus (véase el cuadro).
Los Centros para el Control y la Prevención de Enfermedades (CDC) y la FDA administran conjuntamente el sistema de vigilancia pasiva del Sistema de Notificación de Eventos Adversos a las Vacunas (VAERS), que se utiliza para detectar señales que requieren una investigación más profunda. Pero pocos informes del VAERS incluyen los hallazgos clínicos o de laboratorio específicos necesarios para determinar la causalidad. Hay otras bases de datos gubernamentales de vigilancia activa que sí lo permiten.
En las últimas dos décadas, se han introducido muchas vacunas nuevas para niños y para poblaciones vulnerables, como mujeres embarazadas y adultos mayores. Sin embargo, el presupuesto para el monitoreo de la seguridad de las vacunas en los CDC (que son responsables de la mayoría de los esfuerzos federales de los EE. UU.) se ha estancado durante este período, en alrededor de US$20 millones por año.
Los autores consideran que la vigilancia postautorización podría financiarse con el fondo que se ha creado para compensar a los que experiementan eventos adversos por las vacunas, que suele tener superávit, y en 2023 contaba con US$4.300 millones.
Fuente Original