En mayo de 2024, la gran empresa farmacéutica AstraZeneca anunció que retiraría del mercado mundial su vacuna contra la covid-19 basada en vector de adenovirus, la cual había desarrollado en colaboración con la Universidad de Oxford.
Cuando surgió por primera vez como candidata a vacuna a finales de 2020, fue aclamada como un hito en la lucha contra la pandemia.
Pero en los años siguientes, la vacuna se enfrentó a numerosas dudas sobre su eficacia, régimen de administración y seguridad.
Se han planteado preguntas válidas sobre cómo fue posible que la vacuna contra la covid-19 de AstraZeneca llegara a comercializarse. Así que he decidido echar un vistazo a su evolución.
Afirmaciones exageradas
La vacuna de AstraZeneca fue autorizada en el Reino Unido, Europa, Asia y Australia.
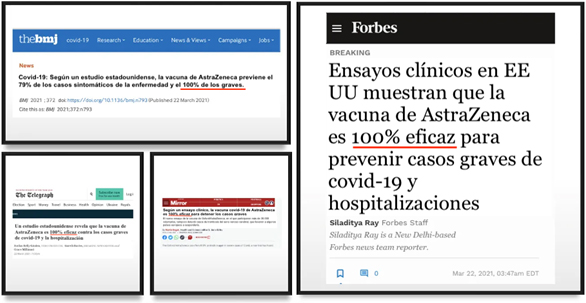
En febrero de 2021, AstraZeneca se jactó en un comunicado de prensa de que los primeros resultados de su ensayo clínico de fase III demostraron que la vacuna podía proporcionar una protección del 100% contra los casos graves de la enfermedad, la hospitalización y la muerte [1].

La noticia se divulgó por todos lados. Desde periódicos sensacionalistas hasta revistas médicas, todo el mundo estaba ansioso por informar sobre este extraordinario hallazgo que la empresa farmacéutica había mencionado en su comunicado de prensa.
Los políticos se unieron al coro.
El entonces ministro de salud australiano, Greg Hunt, se presentó ante la prensa para dar fe de la seguridad de la vacuna y animó a la gente a ponérsela [2].
El primer ministro, Scott Morrison, afirmó que los australianos podían tener “absoluta confianza” en la vacuna y se mostró entusiasmado por el hecho de que se fabricaran más de 50 millones de dosis en una instalación local de Melbourne [3, 4].
Pero ¿era demasiado buena para ser verdad?
En una inesperada amonestación, el Comité de Supervisión de Seguridad de Datos (DSMB o Data Safety Monitoring Board), que se encargaba de supervisar el ensayo clínico, reprendió a AstraZeneca por hacer públicos datos “seleccionados por conveniencia”, que podrían haber dado la impresión de que la vacuna era más eficaz que lo que en realidad era [5].
“Decisiones como esta son las que merman la confianza del público en el proceso científico”, comentó el Comité de Supervisión de Seguridad de Datos.
El Comité de Supervisión de Seguridad de datos también escribió a la agencia de Anthony Fauci, los Institutos Nacionales de Salud (NIH o National Institutes of Health) [6], preocupado porque AstraZeneca había hecho pública “información desactualizada de ese ensayo, que pudo haber proporcionado una visión incompleta de los datos sobre la eficacia de la vacuna”.
Pero Fauci restó importancia a las preocupaciones diciendo a millones de espectadores en Good Morning America (Buenos Días América) que se trataba simplemente de “una equivocación” de AstraZeneca, y que el Comité de Supervisión de Seguridad de Datos estaba siendo “bastante duro”.
“Es realmente lamentable que esto haya sucedido”, dijo Fauci a los telespectadores [7]. “El hecho es que es muy probable que se trate de una vacuna muy buena, y este tipo de cosas… realmente arrojan algunas dudas sobre las vacunas y quizá contribuyen a la indecisión. No era necesario”.
Aparecen los coágulos de sangre
Poco después del lanzamiento de la vacuna empezaron a aparecer signos preocupantes.
Los sistemas de vigilancia europeos detectaron casos graves de una enfermedad de coagulación sanguínea llamada trombosis con trombocitopenia (STT) tras la vacunación, que estaban causando discapacidad grave, hospitalización y muerte.
Austria fue el primer país en actuar.
El 7 de marzo, las autoridades austriacas anunciaron que suspenderían un único lote de la vacuna de AstraZeneca [8], después de que dos mujeres (de 35 y 49 años) desarrollaran graves coágulos sanguíneos; una de ellas falleció.
Cuatro días después, tres países nórdicos —Dinamarca, Noruega e Islandia— suspendieron por completo la vacuna de AstraZeneca [9], hasta que se pudieran obtener más datos sobre su seguridad.
Uno por uno, los países europeos empezaron a abandonar la vacuna [10]: Alemania, Francia, España, Estonia, Lituania, Luxemburgo, Italia y Letonia.
Se estaba produciendo un desastre de relaciones públicas.
Gestión de la crisis
Todos, desde los responsables políticos hasta los medios de comunicación y las sociedades académicas, entraron en acción para minimizar las dudas sobre la vacuna.
John Skerritt, jefe de la Agencia Reguladora de Medicamentos de Australia, la Administración de Bienes Terapéuticos (TGA o Therapeutic Goods Administration), declaró en la radio de Sydney que su agencia “no había encontrado ninguna evidencia de estos coágulos” entre los australianos [11].
Paul Kelly, director médico australiano, afirmó que “no había pruebas de que causara coágulos sanguíneos”, y el primer ministro Morrison dijo que no había recibido “ningún consejo para pausar el lanzamiento en Australia” [12, 13].
En medio de toda la publicidad sobre los coágulos sanguíneos, AstraZeneca anunció su intención de reclutar a un nuevo “Especialista en Comunicaciones” que ayudara a transformar la narrativa negativa en positiva.

AstraZeneca también inició colaboraciones con celebridades internacionales como el músico y ganador de un Oscar, Jeff Bridges, que participó en la campaña “Up The Antibodies” (“Arriba los anticuerpos”) para fomentar la vacunación y otros tratamientos de AstraZeneca [14].
La Academia Australiana de Ciencias anunció que, después de vacunarse, el riesgo de muerte por trombosis con trombocitopenia (STT) era de “uno en un millón”, y que era más probable que te cayera un rayo que morir de esa enfermedad [15].

Sin embargo, poco pudo hacer para frenar el flujo de informes de personas que estaban muriendo por coágulos sanguíneos graves, poco después de la vacunación.
En mayo de 2021, la agencia reguladora de medicamentos del Reino Unido informó sobre 242 casos de coágulos y 49 muertes, tras la inyección con la vacuna de AstraZeneca [16], lo que llevó al Comité Conjunto de Vacunación e Inmunización (JCVI o Joint Committee no Vaccination and Immunisation) a recomendar que se ofreciera una vacuna alternativa a los menores de 40 años.
El gobierno australiano actualizó discretamente los formularios de “consentimiento informado” que se entregaban a las personas que se querían vacunar, para incluir preguntas sobre sus antecedentes de coágulos sanguíneos.
El Grupo Australiano de Asesoramiento Técnico sobre Inmunización (ATAGI o Australian Technical Advisory Group on Immunisation) cambió sus recomendaciones y propuso que la vacuna se limitara a las personas mayores de 50 años [17].
Dos meses después, el ATAGI elevó [18] el límite de edad a por encima de los 60 años.
Ensayo clínico corrupto
El ensayo clínico de fase III de AstraZeneca fue controvertido desde el principio. Se llevó a cabo en varios centros de investigación, y los participantes estuvieron en protocolos diferentes [19].
Algunos participantes recibieron una dosis, otros dos. Algunos recibieron placebos de solución salina, mientras que otros recibieron la vacuna meningocócica (MenACWY) como placebo, además de paracetamol para ayudar a “cegar” a los participantes.
Esto dificultó la evaluación de los efectos adversos de todo el ensayo y también dio lugar a errores de dosificación, ya que algunos participantes recibieron dosis más bajas de la vacuna que otros [20].
Para acabar de complicar las cosas, AstraZeneca tuvo que explicar por qué los que recibieron una dosis más baja de la primera inyección estaban mejor protegidos contra la infección que los que recibieron dos dosis completas [21].
Cuando por fin se publicaron los resultados del ensayo clínico en la revista médica, New England Journal of Medicine, uno de los participantes delató a los investigadores [22].
Brianne Dressen participó en el ensayo y se sintió mal casi inmediatamente después de su primera dosis. Empezó a sentir hormigueos y pinchazos en el brazo derecho, un trastorno denominado parestesia, el cual se extendió al brazo izquierdo y a otras partes del cuerpo
Esa misma noche aparecieron otros síntomas progresivamente preocupantes, como visión borrosa, visión doble, dolor de cabeza, sensibilidad al sonido, un fuerte zumbido en los oídos (tinnitus), náuseas, vómitos, fiebre y escalofríos.
Los investigadores la retiraron del ensayo y desactivaron la aplicación de su teléfono inteligente con la que registraba todos sus síntomas, borrando así sus registros.
La publicación del ensayo en el New England Journal of Medicine tampoco incluía información sobre los daños que le había causado la vacuna, y cuando Dressen pidió al redactor jefe de la revista, Eric Rubin, que corrigiera la publicación para incluir sus datos, este se negó [23].
Demandas en curso
En marzo de este año, docenas de pacientes y familiares iniciaron acciones legales contra AstraZeneca en la Corte Suprema del Reino Unido, después de que la vacuna terminara con la vida de sus seres queridos o les dejara secuelas catastróficas por STT [24].
Jaime Scott es el principal demandante, quien sufrió un daño cerebral permanente por un coágulo de sangre, tras recibir la vacuna de AstraZeneca en abril de 2021.
El caso se ha presentado bajo la Ley de Protección al Consumidor del Reino Unido, para eludir la inmunidad legal que el Gobierno británico concedió a AstraZeneca en el momento en que se aprobaron las vacunas.
Los documentos judiciales de este caso revelan que AstraZeneca ha admitido que su vacuna contra la covid-19 puede, en casos muy raros, causar STT [25].
También en mayo de este año, Dressen presentó una demanda contra AstraZeneca, después de que la empresa se negara a cubrir sus gastos hospitalarios y las crecientes facturas médicas [26].
El formulario de consentimiento que firmó antes de participar en el ensayo clínico estipulaba que la empresa “cubriría los costes de los daños ocasionados por la investigación” y que “pagaría los gastos del tratamiento médico” [27].
Dado que AstraZeneca se ha negado a cumplir sus obligaciones, Dressen está buscando daños económicos y emocionales pasados y futuros.
Adiós a la vacuna
En octubre de 2021, casi 12,5 millones de dosis de la vacuna de AstraZeneca se habían administrado a australianos.
Pero los temores persistentes de coágulos sanguíneos potencialmente mortales llevaron a las autoridades a recomendar otras marcas de vacunas contra la covid-19 (Pfizer y Moderna).
La fabricación de la vacuna de AstraZeneca en Australia cesó a finales de 2021, y en marzo de 2023 ya no estaba disponible [28].
Hasta la fecha, la Administración de Bienes Terapéuticos de Australia afirma que la incidencia de STT, tras la vacuna de AstraZeneca, es de 1 entre 50.000.
A pesar de que se notificaron más de 1.000 muertes a la Administración de Bienes Terapéuticos tras la vacunación contra la covid-19, solo 13 muertes se han atribuido a la vacuna de AstraZeneca.
En 2021, se presentó una solicitud de libertad de información a la Administración de Bienes Terapéuticos, pidiendo detalles de su investigación sobre las más de 1.000 muertes notificadas, pero la agencia denegó la solicitud, lo que plantea serias dudas de que alguna vez se llevara a cabo una investigación exhaustiva e independiente sobre las muertes relacionadas con la vacuna covid-19 en Australia.
Referencias