A continuación, resumimos una nota publicada en BioPharma Dive [1] sobre como Amgen extendió su monopolio sobre Enbrel (etanercept) por tres décadas a través de una maraña de patentes.
Enbrel no es el primer medicamento de grandes ventas de Amgen. Epogen (eritropoyetina) y Neupogen (filgrastim) también fueron medicamentos de grandes ventas, antes de que caducaran sus patentes en EE UU, alcanzaron un total de US$45.000 millones y US$25.000 millones respectivamente. Sin embargo, Enbrel será el que más beneficios le aporte, gracias a la maraña de patentes que lo protege, se calcula que las ventas acumuladas para 2029 podrían llegar a alcanzar los US$100.000 millones, una cifra solo alcanzada por unos pocos medicamentos a lo largo de la historia.
No se podrán aprobar competidores de etanercept hasta el 2029, 37 años después de que se solicitara la primera patente para Enbrel y 17 años después de que ésta haya expirado. Sin competencia de genéricos, Amgen puede fijar su precio en niveles muy altos, el precio de lista de un tratamiento anual en 2017 en EE UU era de US$53.000.
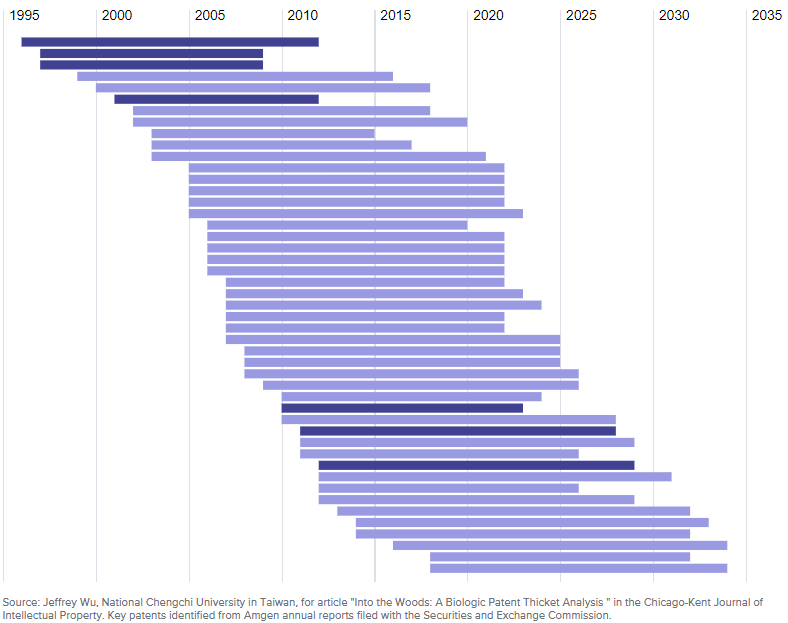
El gráfico a continuación ilustra las patentes que Amgen utilizó para proteger a Enbrel durante más de 30 años. Las barras en azul oscuro indican las siete patentes cruciales que le han permitido mantener el poder del monopolio evitando el ingreso de los biosimilares.
La historia de Enbrel tiene sus particularidades, el descubrimiento original lo realizó Bruce Beutler, quien luego ganó el premio Nobel, y obtuvo su primera patente. Su institución cedió la licencia sobre el prometedor producto a una compañía biotecnológica llamada Immunex en 1995. Tres años más tarde, la FDA aprobó Enbrel, lo que puso a Immunex en apuros, pues no tenía suficiente capacidad de producción.
Después de aumentar su capacidad de producción, e incluso de tercerizar una parte en otros laboratorios, Inmunex no se preocupó mucho por patentar los procesos de producción, algo que después hizo Amgen. Pero si tomó una decisión crucial en materia de patentes. En 1999, adquirió los derechos de Roche sobre un método para fabricar una proteína de fusión que bloquea el TNF. La farmacéutica suiza había solicitado la patente en 1990, pero aún no se la habían concedido. Esto resultó ser un golpe de suerte, ya que acabaría siendo la última defensa contra futuros rivales.
En 2001 la compañía fue adquirida por Amgen, en uno de los acuerdos más importantes en la historia de la biotecnología, los abogados de Amgen empezaron a patentar los procesos de fabricación y formulación, métodos de uso y dispositivos de administración. En total Amgen logró obtener al menos 68 patentes para Enbrel, y en documentos que ha presentado ante la Comisión de Bolsa y Valores, Amgen identifica a las siete patentes principales. Cuatro de ellas, incluyendo la patente original de Beutler, han expirado, pero quedan tres.
La más importante es la licencia sobre la propiedad intelectual que Immunex obtuvo de Roche en 1999 y que finalmente logró patentar en 2012.
La forma en que esa invención en particular extendió la exclusividad de Enbrel se debe a una peculiaridad del derecho internacional de patentes. Como Roche presentó la solicitud antes de que entrara en vigor el acuerdo de la Organización Mundial del Comercio sobre derechos de patente conocido como ADPIC, la patente recibió 17 años de protección desde la fecha de publicación. Si se hubieran aplicado a esa solicitud las normas del ADPIC, la patente habría expirado en 2010.
Tahir Amin, fundador de I-MAK dijo que el lapso de 22 años transcurrido entre la primera solicitud de Roche y la eventual concesión de la patente refleja también la forma en que la ley de patentes de Estados Unidos favorece la concesión de monopolios a las empresas. Las solicitudes de patentes pueden mantenerse vivas durante muchos años presentando documentos que amplíen la invención original, así como solicitando una nueva revisión cuando se rechaza una patente. En cambio, en Europa, si se rechaza una patente sólo se puede recurrir dos veces.
Mientras Amgen construía este muro de patentes, el gobierno de EE UU alentaba a que las empresas produjeran genéricos y biosimilares para conseguir precios más accesibles. En 2010, el Congreso aprobó la Ley de Competencia e Innovación de Precios de Productos Biológicos (BPCIA). La ley facilitó la aprobación de los biosimilares. Lamentablemente, no ha tenido el impacto esperado, en parte por las marañas de patentes que protegen los monopolios.
Enbrel, que por aquel entonces tenía ventas de US$3.000 millones al año, podría enfrentar la competencia de los biosimilares. La división Sandoz de Novartis comenzó a desarrollar una copia de Enbrel en 2012 y, cuatro años después, obtuvo la aprobación de la FDA para Erelzi, el tercer biosimilar autorizado por la agencia. Sin embargo, cinco años después, Erelzi aún no se ha comercializado, La maraña de patentes de Amgen se interpone en el camino de Erelzi y del biosimilar Eticovo de Samsung Bioepis, aprobado posteriormente. Amgen llevo el caso de Erelzi a los tribunales y Sandoz dijo que la propiedad intelectual era la misma que la de otras patentes que habían caducado. Amgen ganó en primera y segunda instancia, pero Novartis apeló a la Corte Suprema, que desestimó el caso cerrando todas las posibilidades legales.
La situación podría cambiar en los próximos años ya que la administración Biden ha dicho que las agencias federales deberán analizar mejor las marañas de patentes. Tanto la FDA como la Oficina de Patentes y Marcas Registradas de EE UU (USPTO) han comenzado a favorecer el desarrollo de biosimilares.
En Europa la historia es muy diferente, los biosimilares de Enbrel se comercializan desde 2016 y tienen una participación en el mercado cercana al 40%. Amgen no comercializa Enbrel allí, sino que lo hace su socio Pfizer, quien declaró haber reducido sus ventas en casi US$300 millones desde 2019, debido a la continua competencia de los biosimilares.
Fuente original:
Nota de Salud y Fármacos. El 1 de diciembre, Kansteiner publicaba en Fiercepharma (Amgen stalls Samsung’s Enbrel biosim until 2029 in 2nd patent win of the year https://www.fiercepharma.com/pharma/amgen-stalls-samsung-s-enbrel-biosim-until-2029-second-patent-win-year) informando que después de que en mayo 2021 la Corte Suprema se negara a revisar una disputa de patentes de Sandoz contra Enbrel; en diciembre 2021, un tribunal de distrito de Nueva Jersey se puso de lado de Amgen, Roche e Inmunex, por lo que Samsung Bioepris no podrá comercializar su biosimilar de Embrel, Eticovo, en EE UU hasta 2029, cuando expiran las patentes. Enbrel se aprobó por primera vez en 1998, lo que significa que habrá disfrutado de 31 años de exclusividad en los EE UU para cuando los biosimilares de Samsung (Eticovo) y Sandoz (Erelzi) entren en escena
El artículo publicado en FiercePharma añade: La Ley de innovación y competencia de precios de productos biológicos de 2009 otorga a los nuevos productos biológicos 12 años de exclusividad a partir de su aprobación por la FDA, agregó el Centro de biosimilares. Erelzi fue aprobado en 2016 y Eticovo en 2019. Los litigios de patentes los han mantenido fuera del mercado desde entonces, a medida que el reloj de la exclusividad sigue corriendo.
La mayoría de las ventas de Enbrel están en EE UU. En todo el mundo, el medicamento generó US$$4.990 millones en 2020, de los cuales US$4.850 millones provienen de los EE. UU. Pfizer comercializa el medicamento en Europa, donde Samsung, Sandoz y Viatris venden versiones biosimilares.