Los ensayos controlados de fase III se consideran la “norma de oro” para evaluar la eficacia y la seguridad de las vacunas en humanos.
Estos son los ensayos en los que se han basado las autoridades para asegurar al público que las vacunas covid-19 son “seguras y eficaces”.
Se sabe que las vacunas aportan beneficios porque reducen la gravedad de la enfermedad y las hospitalizaciones, pero ¿qué sabemos de sus efectos adversos?
La información sobre los efectos adversos es vital para que los reguladores, los responsables políticos, los médicos y los pacientes puedan tomar buenas decisiones.
Sin embargo, hay una gran preocupación por el sesgo de publicación u omisión selectiva de datos, que disminuye la probabilidad de que se publiquen los acontecimientos adversos y se enfatice la publicación de los resultados positivos.
Una revisión sistemática publicada en la revista PLOS [1] analizó 28 estudios y descubrió que era menos probable que los acontecimientos adversos aparecieran en los artículos publicados en las revistas que en los estudios no publicados (por ejemplo, los datos que tiene la industria).
Ahora, los expertos sugieren que los ensayos pivotales de la vacuna covid-19 podrían haber subestimado los acontecimientos adversos de varias maneras.
Seguimiento virtual con aplicaciones digitales
En los ensayos de las vacunas de Pfizer y AstraZeneca se dotó a los participantes con aplicaciones digitales para informar los efectos adversos a distancia, una forma de recopilar datos de los pacientes que es más cómoda, requiere menos tiempo y es más rentable que cuando tienen que acudir a los centros de investigación.
Sin embargo, un problema importante es que las opciones predeterminadas de las aplicaciones digitales se centran únicamente en determinados acontecimientos adversos.
Por ejemplo, la aplicación sólo permite que los participantes registren lo que la empresa considera acontecimientos “esperados”, como fiebre, dolor o calor en el lugar de la inyección, enrojecimiento, hinchazón, fatiga, dolor de cabeza, diarrea, escalofríos, dolor muscular y articular.
Pero si experimentan un acontecimiento adverso grave, como miocarditis o signos tempranos de mielitis transversal, síndrome de Guillain-Barré, un trastorno miopático, miocarditis o trombosis, la aplicación no incluye una opción para registrarlo.
Un ejemplo: Brianne Dressen, participante en el ensayo de AstraZeneca (AZD1222) sufrió un acontecimiento adverso grave tras recibir la primera dosis y quedó incapacitada.
Pero la aplicación de su smartphone no le permitía registrar el tipo concreto de acontecimiento adverso, ni tampoco informar sus síntomas con sus propias palabras.
Una vez hospitalizada, se desenmascaró a la Sra. Dressen del ensayo. Se le informó de que se le había administrado la vacuna de AstraZeneca, no el placebo, y se le aconsejó que no se pusiera la segunda dosis.
Posteriormente, los investigadores “retiraron” a la Sra. Dressen del ensayo, desactivaron la aplicación de su smartphone y a partir de ese día se dejaron de documentar todos sus datos, a pesar de que sigue teniendo una discapacidad.
La Sra. Dressen estaba preocupada por la falta de información sobre su acontecimiento adverso (y otros) en la publicación de ese ensayo en el prestigioso New England Journal of Medicine [2].
Escribió a la revista para “pedir que se corrigieran las inexactitudes en la publicación del ensayo y exigir que se incluyera toda la información y los resultados del ensayo”.
El redactor jefe, el Dr. Eric Rubin, se negó a corregir la información inexacta que se publicó en su revista. El intercambio de correos electrónicos se ha divulgado al público [3].
Si los fabricantes de vacunas retiran selectivamente a los sujetos que experimentan efectos adversos graves (como en el caso de Brianne Dressen y otros) es fácil entender que los ensayos encontraron en su mayoría aumentos “estadísticamente significativos” de efectos adversos leves (fiebre, escalofríos, dolores de cabeza), pero no de los daños graves.
Culpar a una enfermedad subyacente
Cuando Pfizer reclutó a jóvenes de 12 a 15 años para su ensayo de la vacuna de ARNm, los datos que se publicaron en el New England Journal of Medicine [4], afirmaban que no había habido “ningún acontecimiento adverso grave relacionado con la vacuna”.
Una de las participantes en el ensayo fue Maddie De Garay, de 13 años. Fue asignada aleatoriamente al grupo que recibió la vacuna y, tras recibir su primera dosis, Maddie sufrió una grave reacción adversa que la dejó en una silla de ruedas y alimentada por una sonda nasogástrica.
Fue remitida al hospital para que le hicieran una evaluación completa y un médico le diagnosticó un “trastorno funcional”.
En pocas palabras, este médico decidió que la culpa de su discapacidad física era una predisposición a la “histeria”, y no la vacuna, y sobre esta base la remitió a un centro de salud mental.
El Dr. David Healy, psiquiatra residente en Ontario (Canadá), revisó exhaustiva del historial médico de la niña Maddie, se entrevistó con la familia, y no encontró ningún antecedente de afecciones preexistentes ni de enfermedad mental.
“Haberle atribuido esta designación en el ensayo clínico no sólo es erróneo, sino bastante increíble”, dijo el Dr. Healy, que temía que el diagnóstico erróneo pusiera en peligro el tratamiento y el progreso de Maddie.
“Podría ser incluso sociopático, ya que parece que, para mantener la posición de Pfizer, esta joven no está recibiendo el tratamiento que normalmente se indicaría para los problemas que tiene. En su lugar, basándose en un supuesto ‘trastorno funcional’, se la ha dirigido a un centro de salud mental”, dijo el Dr. Healy.
“Si hay alguna posibilidad de que tenga una enfermedad preexistente, entonces no culpan a la vacuna”, dice. “Y así pueden afirmar que no hubo eventos graves relacionados con la vacuna porque no creen que su reacción estuviera ‘relacionada con la vacuna’. Es increíble”.
El Dr. Healy dice que lo ha visto antes, en el estudio 329 [5], que analizaba los antidepresivos (ISRS) en niños y adolescentes. Un chico de 15 años fue retirado del ensayo tras serle diagnosticada una “enfermedad intercurrente”.
Más tarde, el Dr. Healy descubrió por casualidad que el participante en el ensayo había desarrollado comportamientos homicidas dos semanas después de tomar el ISRS, lo que, según el Dr. Healy, fue inducido casi con toda seguridad por el fármaco.
Pero como el joven fue diagnosticado con una “enfermedad intercurrente” durante el ensayo, los investigadores no tuvieron que explicar por qué retiraron a este paciente del ensayo.
En el ensayo de fase III de AstraZeneca sobre su vacuna, en el que participó Brianne Dressen, el estudio decía [2]:
“Las muertes que se adjudicaron como no relacionadas con covid-19 se trataron como acontecimientos intercurrentes y, por tanto, se censuraron en la fecha de la muerte”.
El Dr. Healy afirmó: “Es muy posible que se trate de un sumidero por el que se han desvanecido las muertes causadas por la vacuna. Los pacientes con accidentes cerebrovasculares, infartos de miocardio o episodios trombóticos pueden haberse incluido ahí, con la justificación de que debían tener un corazón dudoso u otra enfermedad preexistente [o intercurrente].”
Muertes relacionadas con la vacuna
El Dr. Healy señala que, al publicar las muertes en los ensayos, los investigadores no relacionan la vacuna con las muertes que se producen inmediatamente después de la primera dosis de la vacuna, sino hasta que hayan transcurrido hasta 14 días después de la segunda dosis.
En otras palabras: 1) primera dosis, 2) esperar tres semanas antes de la segunda dosis, 3) esperar otras dos semanas. Es decir, hay un total de cinco semanas durante las que no se considera que las muertes estén relacionadas con la vacuna.
Los investigadores dicen que esto se debe a que los participantes no son “totalmente inmunes” hasta dos semanas después de la segunda dosis. Esto es cierto.
Sin embargo, no captan las muertes que podrían haber causado las vacunas en ese periodo de cinco semanas.
El Dr. Healy fue muy crítico con este método de recogida de datos.
“Se supone que los ensayos controlados aleatorios no permiten tomar decisiones como ésta. Se deberían notificar todas las muertes. La empresa puede decir que no cree que las muertes se deban a la vacuna, pero necesitamos tener la oportunidad de saber cuántas fueron y decidir si es necesario investigarlas más”, dijo el Dr. Healy.
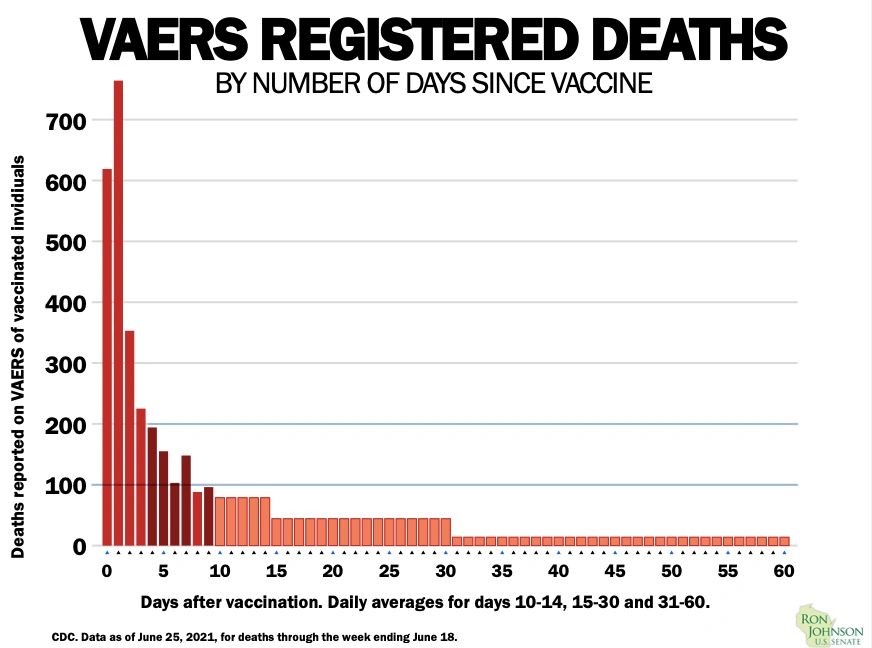
Es importante saberlo porque los datos del mundo real que tiene el CDC (a fecha de 25 de junio de 2021) muestran que la mayoría de las muertes notificadas tras recibir una vacuna Covid-19 se producen en un plazo de 30 días.
Estos datos de vigilancia no pueden establecer una relación causal con la vacuna, pero la señal se considera significativa, especialmente si las muertes relacionadas con la vacuna no se están captando en los ensayos controlados.
La lección de los “ensayos controlados”
Los datos sobre la seguridad de las vacunas son tan importantes como los de eficacia, aunque los medios de comunicación y los funcionarios de salud pública suelen centrarse en estos últimos.
Hasta ahora, los informes sobre los acontecimientos adversos graves y potencialmente mortales relacionados con las vacunas no se han detectado en los ensayos controlados “de referencia”. Sólo se han identificado tras vacunar a cientos de miles de personas.
La miocarditis, por ejemplo, sólo surgió en Israel cuando se empezó a distribuir la vacuna de Pfizer entre la población. Y los informes de trombocitopenia trombótica inducida por la vacuna (VITT), relacionada con la vacuna de AstraZeneca surgieron primero de los sistemas de vigilancia europeos, no de los ensayos controlados.
Si todos los ensayos de la vacuna Covid-19 son financiados, diseñados, realizados y analizados por los fabricantes -que se sabe que distorsionan los resultados para favorecer los objetivos del patrocinador-, habría que hacer un mayor esfuerzo para obtener acceso a los datos y permitir un escrutinio independiente.
Referencias